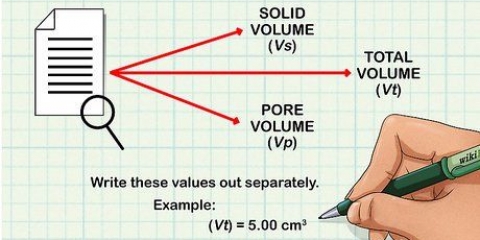
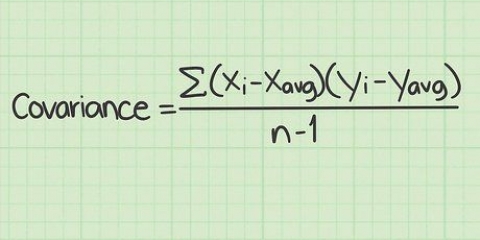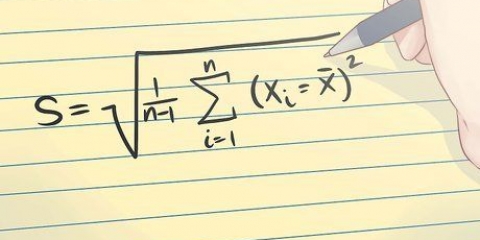Die gemete absorpsie tussen verskillende lesings kan verskil as gevolg van die konsentrasie van die oplossing en die vorm van die houer wat gebruik word om die intensiteit te meet. Molêre absorpsie kompenseer vir hierdie variasies. 
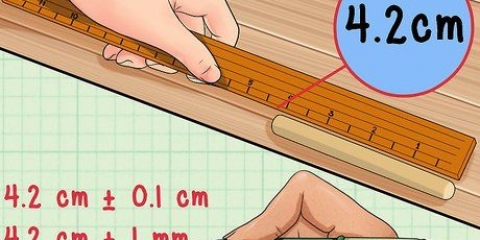
Berei `n oplossing met `n bekende konsentrasie, c, vir ontleding. Die eenheid van konsentrasie word gegee in mol of mol/liter. Om l om te vind, meet die lengte van die kuvet. Die eenheid vir die lengte van die pad is sentimeter. Gebruik `n spektrofotometer om absorpsielesing te verkry a by `n gegewe golflengte. Die eenheid vir golflengte is meter, maar die meeste golflengtes is so klein dat hulle eintlik in nanometer (nm) gemeet word. Absorbansie het geen eenheid nie. 
Byvoorbeeld: met `n 1 cm-kuvet meet jy die absorpsie van `n oplossing met `n konsentrasie van 0,05 mol/L. Die absorpsie by `n golflengte van 280 nm is 1,5. Wat is die molêre absorpsie van hierdie oplossing?? ɛ280 = A/lc = 1.5/(1 x 0.05) = 30 L mol cm 

Trek `n lyn tussen elk van die punte. As die metings korrek is, moet die punte `n reguit lyn vorm wat aandui dat die absorpsie en konsentrasie ooreenstem met Beer se wet. 
Die vergelyking van die helling of helling van `n lyn is (Y2 - Y1)/(X2 - X1). Die punt hoër op die lyn kry 2 as onderskrif en die laagste punt kry 1 as onderskrif. Byvoorbeeld, die absorpsie by `n molêre konsentrasie van 0.2 is 0.27 en by `n molêre konsentrasie van 0.3 is die absorpsie 0.41. Die waardes van die absorpsie is Y-waardes, terwyl die konsentrasies X-waardes is. Deur die vergelyking van `n lyn te gebruik, bereken ons: (Y2 - Y1)/(X2 - X1) = (0.41-0.27)/(0.3-0.2) = 0.14/0.1 = 1.4 is die helling van die lyn. 
Om ons voorbeeld voort te sit: as 1.4 die helling van die lyn is en die padlengte 0.5 cm is, dan is die molêre absorpsie 1.4/0.5 = 2.8 L mol cm.
Bereken molêre absorpsie
Inhoud
Molêre absorpsie, ook bekend as die molêre uitsterwingskoëffisiënt, is `n maatstaf van die absorpsie van `n bepaalde golflengte van lig deur `n chemikalie. Dit laat jou toe om vergelykings tussen verbindings te tref sonder om die verskille in konsentrasie of oplossinglengte tydens metings in ag te neem. Dit word dikwels in chemie gebruik en moet nie met die uitsterwingskoëffisiënt verwar word nie, aangesien dit gewoonlik in fisika gebruik word. Die standaard eenhede vir molêre absorpsie is liter per mol sentimeter (L mol cm).
Trappe
Metode 1 van 2: Bereken die molêre absorpsie met `n vergelyking

1. Verstaan Beer-Lambert se wet vir uitsterwing, A = lc. Die standaardvergelyking vir absorpsie is A = lc, waar a verteenwoordig die hoeveelheid lig wat deur die monster geabsorbeer word vir `n gegewe golflengte, ɛ is die molêre absorpsie, l is die afstand wat lig deur die oplossing beweeg, en c is die konsentrasie van die absorpsiemiddels per volume-eenheid.
- Absorpsie kan ook bereken word deur die verhouding tussen die intensiteit van `n verwysingmonster en die onbekende monster te gebruik. Dit word deur die vergelyking gegee A = log10(EkO/I).
- Die intensiteit kan met `n spektrofotometer verkry word.
- Die absorpsie van `n oplossing verander na gelang van die golflengte in die oplossing. Sommige golflengtes sal meer geabsorbeer word as ander, afhangende van die samestelling van die oplossing. Moenie vergeet om te noem watter golflengte jy vir die berekening gebruik nie.

2. Herrangskik die Beer-Lambert-vergelyking om die molêre absorpsie op te los. Deur algebra te gebruik, kan ons die absorpsie deur die lengte en die konsentrasie deel, om die molêre absorpsie aan die een kant van die vergelyking te isoleer: ɛ = A / lc. Nou kan ons hierdie basiese vergelyking gebruik om die molêre absorpsie vir `n gegewe golflengte te bereken.

3. Kry die waardes vir die veranderlikes in die vergelyking met behulp van spektrofotometrie. `n Spektrofotometer is `n toestel wat `n spesifieke golflengte van lig deur `n stof stuur en bespeur hoeveel lig weer uitkom. Van die lig sal deur die oplossing geabsorbeer word en die oorblywende lig wat oorgedra word kan gebruik word om die absorpsie van hierdie oplossing te bereken.

4. Pas die waardes van die veranderlikes toe op die molêre absorpsievergelyking om op te los. Gebruik die waardes waarvoor u verkry is a, c en l, vul die vergelyking in ɛ = A / lc in. Vermenigvuldig l van c en deel a dan deur die produk, om die molêre absorpsie te kry.
Metode 2 van 2: Bereken die molêre absorpsie deur die beste oplossing te gebruik

1. Meet die intensiteit van oorgedrade lig deur verskillende konsentrasies van `n oplossing. Maak drie of vier konsentrasies van `n oplossing. Gebruik `n spektrofotometer om die absorpsie van `n oplossingkonsentrasie by `n gegewe golflengte te meet. Begin met die laagste konsentrasie van die oplossing en werk jou pad op na die hoogste. Die volgorde is nie belangrik nie, maar dit is belangrik watter absorpsie by watter berekening hoort.

2. Stip die konsentrasie teen die absorpsie op `n grafiek. Gebruik die waardes wat met die spektrofotometer verkry is om a grafiek. Vir elke individuele waarde plaas die konsentrasie op die x-as en die absorpsie op die y-as.

3. Besondergradiënt van die lyn van die beste passing, deur die punte op die grafiek te gebruik. Om die helling van die lyn te bereken, deel die absorpsie deur die konsentrasie. Gebruik twee van jou grafiekpunte, trek die X- en Y-waardes af, en bereken dan Y/X.

4. Verdeel die helling van die lyn deur die lengte van die pad (die diepte/breedte van die kuvet) om die molêre absorpsie te bereken. Die laaste stap vir die berekening van die molêre absorpsie met datapunte is deling deur die lengte van die pad. Dit is die diepte van die kuvet soos dit in die spektrofotometer gebruik word.
Artikels oor die onderwerp "Bereken molêre absorpsie"
Оцените, пожалуйста статью
Gewilde