As jy die besonderhede van jou element ken, soos in watter groep of tydperk dit is, is dit makliker om te vind. As jy niks van die element self weet nie, soek net die tabel vir die ooreenstemmende simbool totdat jy dit kry. 
Byvoorbeeld, die atoomgetal van boor (B) is 5, wat beteken dat dit 5 protone en 5 elektrone bevat. 

Omdat `n elektron `n negatiewe lading het, sal die ioon meer negatief word as jy ekstra elektrone byvoeg. Wanneer jy elektrone verwyder, word die ioon meer positief. Byvoorbeeld, N het `n lading van -3, terwyl Ca `n lading van +2 het. 
Byvoorbeeld, Ca het `n lading van +2 en dus 2 elektrone minder as `n neutrale kalsiumatoom. Die atoomgetal van kalsium is 20, so hierdie ioon het 18 elektrone. 
Byvoorbeeld, N het `n lading van -3, wat beteken dit het 3 meer elektrone as `n neutrale stikstofatoom. Die atoomgetal van stikstof is 7, so hierdie ioon het 10 elektrone.
Bepaling van die aantal elektrone in 'n element
Inhoud
`n Elektron is `n negatief gelaaide deeltjie en is deel van `n atoom. Alle basiese elemente bestaan uit elektrone, protone en neutrone. `n Fundamentele konsep in chemie is die vermoë om te bepaal hoeveel elektrone `n atoom bevat. Dit kan maklik bepaal word deur die periodieke tabel van die elemente te gebruik. Ander belangrike konsepte is die aantal neutrone en valenselektrone (die aantal elektrone in die buitenste dop van `n atoom) in `n element.
Trappe
Metode 1 van 2: Bepaal die aantal elektrone in `n neutrale atoom

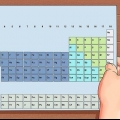
1. Het `n periodieke tabel van die elemente. Dit is `n kleurgekodeerde tabel waarin alle bekende elemente volgens atoomstruktuur georden word. Elke element het `n afkorting van 1, 2 of 3 letters, en word gelys, bykomend tot die atoommassa en atoomgetal.
- In die meeste chemie handboeke sal jy `n periodieke tabel vind (of anders soek aanlyn).

2. Vind die betrokke element in die periodieke tabel. Die elemente word volgens atoomgetal gerangskik en in drie hoofgroepe verdeel: metale, nie-metale en metalloïede (halfmetale). Verder word hulle verder in families gegroepeer, insluitend die alkalimetale, halogene en die edelgasse. Elke kolom van die tabel word `n groep genoem en elke ry `n punt.

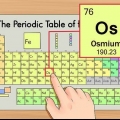
3. Bepaal die atoomgetal van `n element. Die atoomgetal is in die boonste linkerhoek, bo die element se simbool in die blokkie. Die atoomgetal is die aantal protone in `n element. Protone is die deeltjies in `n element met `n positiewe lading. Omdat elektrone `n negatiewe lading het, het `n neutrale element dieselfde aantal protone as elektrone.
Metode 2 van 2: Bepaling van die aantal elektrone in positief/negatief gelaaide ione

1. Bepaal die atoomgetal van `n element. Die atoomgetal is in die boonste linkerhoek; bo die simbool van die element in die boks. Die atoomgetal is die aantal protone in `n element. Protone is die deeltjies in `n element met `n positiewe lading. Omdat elektrone `n negatiewe lading het, het `n neutrale element dieselfde aantal protone as elektrone.
- Byvoorbeeld, die atoomgetal van boor (B) is 5, wat beteken dat dit 5 protone en 5 elektrone bevat.

2. Bepaal die lading van die ioon. Die byvoeging of verwydering van elektrone van `n atoom sal nie sy identiteit verander nie, maar sy lading sal verander. In hierdie gevalle het dit nou `n ioon geword, soos K, Ca of N. Gewoonlik word die lading as boskrif regs van die atoomafkorting getoon.

3. Trek die lading van die atoomgetal af as die ioon positief is. As die lading positief is, het die ioon elektrone verloor. Om te bepaal hoeveel elektrone oor is, trek die lading van die atoomgetal af. In hierdie geval is daar meer protone as elektrone.

4. Voeg die lading by die atoomgetal as die lading negatief is. As die lading negatief is, het die ioon elektrone bygekry. Om te bepaal hoeveel elektrone daar in totaal is, tel die lading by die atoomgetal. In hierdie geval is daar minder protone as elektrone.
Artikels oor die onderwerp "Bepaling van die aantal elektrone in 'n element"
Оцените, пожалуйста статью
Soortgelyk
Gewilde