N = M – n N = getal Neutrone M = atoom mgat n = atoom nnommer 




N = M – n N = getal Neutrone M = atoom mgat n = atoom nnommer
Bepaal die aantal neutrone in 'n atoom
Inhoud
Om die aantal neutrone in `n atoom te bepaal is baie maklik en jy hoef nie eers `n eksperiment daarvoor te doen nie. Om die aantal neutrone in `n atoom of isotoop te bereken, hoef jy net hierdie instruksies te volg.
Trappe
Metode 1 van 2: Vind die aantal neutrone in `n atoom

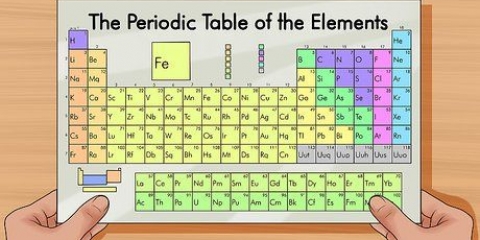
1. Soek die element op die periodieke tabel. In hierdie voorbeeld kyk ons na Osmium (Os), in ry 6.

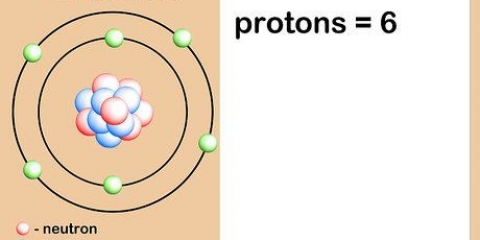
2. Vind die atoomgetal van die element. Dit is gewoonlik die nommer bo die element se simbool. (In die tabel wat ons gebruik is dit die enigste getal.) Die atoomgetal is die aantal protone in een atoom van daardie element. Os het nommer 76, wat beteken dat `n atoom van Osmium 76 protone het.

3. Vind die atoommassa van die element. Dit is gewoonlik die nommer onder die element se simbool. (Dit word nie genoem in die tabel wat ons gebruik nie).Osmium het `n atoommassa van 190,23.

4. Rond die atoommassa af tot die naaste heelgetal om die atoommassa te vind. In ons voorbeeld word 190.23 dan tot 190 afgerond, wat lei tot `n atoommassa van 190 vir Osmium.

5. Trek die atoomgetal van die atoommassa af. Aangesien die meeste van die gewig van `n atoom deur die protone en neutrone opgeneem word, word die aantal protone afgetrek (bv. die atoomgetal) van die atoommassa lewer die aantal neutrone in die atoom Die getalle na die desimale punt verteenwoordig die baie klein massa van die elektrone in die atoom. In ons voorbeeld is dit: 190 (atoommassa) – 76 (aantal protone) = 114 (aantal neutrone).

6. Onthou die formule. Om die aantal neutrone in die toekoms te vind, gebruik die volgende formule:
Metode 2 van 2: Vind die aantal neutrone in `n isotoop

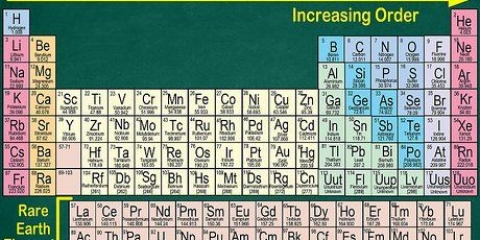
1. Soek die element op die periodieke tabel. As voorbeeld kyk ons na die Koolstof-14-isotoop. Aangesien koolstof-14 `n isotoop van koolstof (C) is, probeer om koolstof in die periodieke tabel (in die tweede ry) te vind.

2. Vind die atoomgetal van die element. Dit is gewoonlik die nommer bo die element se simbool. (In die tabel wat ons gebruik is dit die enigste getal.) Die atoomgetal is die aantal protone in een atoom van daardie element. C is nommer 6 wat beteken dat een koolstofatoom 6 protone het.

3. Vind die atoommassa. Met isotope is dit baie maklik, want hul naam is geneem uit hul atoommassa. Koolstof-14 het byvoorbeeld `n atoommassa van 14. Noudat jy die atoommassa ken, is die hele proses soos om die aantal neutrone in `n gewone atoom te vind.

4. Trek die atoomgetal van die atoommassa af. Aangesien die meeste van die gewig van `n atoom deur die protone en neutrone beset word, word die aantal protone afgetrek (i.e. die atoomgetal) van die atoommassa lewer die aantal neutrone in die atoom. In ons voorbeeld is dit: 14 (atoommassa) – 6 (aantal protone) = 8 (aantal neutrone).

5. Onthou die formule. Om die aantal neutrone in die toekoms te vind, gebruik net die volgende formule:
Wenke
- Osmium, `n metaal wat by kamertemperatuur solied is, kry sy naam van die Griekse woord vir reuk, "osme.”
- As jy ooit onseker is waarvoor `n spesifieke getal in die periodieke tabel staan, onthou dat die tabel gewoonlik rondom die atoomgetal (aantal protone) gebou is, begin by 1 vir Waterstof en opgaan na 118 (Ununoctium). Dit is omdat die aantal protone in `n atoom die atoom bepaal, wat dit die voorkeureienskap van `n element maak vir `n duidelike verdeling. (bv. `n atoom met 2 protone is altyd helium, net soos `n atoom met 79 protone altyd goud is.)
Artikels oor die onderwerp "Bepaal die aantal neutrone in 'n atoom"
Оцените, пожалуйста статью
Gewilde