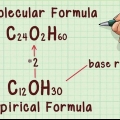
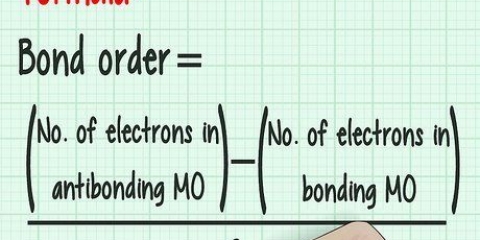
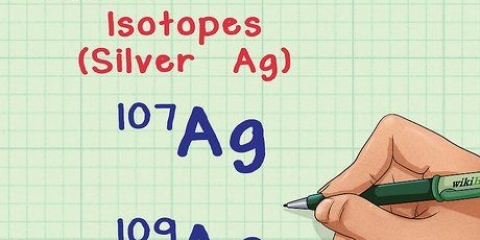Vir koolstofdioksied (CO2) die relatiewe atoommassa is 12,011 amu vir koolstof en 15,999 vir suurstof. Die atoommassa van `n element is ongeveer gelyk aan die som van die massa van die aantal protone en neutrone wat dit bevat. Let daarop dat die relatiewe atoommassa wat jy in die periodieke tabel vind, geskaal is: dit neem alle isotope van die element in die proporsies in ag soos hulle natuurlik voorkom. 
In ons voorbeeld van koolstofdioksied is die massa van die koolstofatoom 12 011 amu. Aangesien daar twee suurstofatome is, skryf dit as  .
. 
Rond die antwoord af waar nodig, deur beduidende syfers te gebruik. Moenie vergeet om die regte eenhede te gebruik nie. amu is die ou afkorting vir atoommassa-eenheid, maar `n beter, moderne eenheid is `n klein geskrewe jy. Vir koolstofdioksied kan die molekulêre massa soos volg gevind word:  .
. 





Berekening van molekulêre massa
Inhoud
Molekulêre massa, voorheen molekulêre gewig (MW) genoem, is die massa van alle atome in `n gegewe molekulêre formule.Molekulêre massa word gemeet in atoommassa-eenhede, gewoonlik uitgedruk in jy of vermaak. Om die molekulêre massa van `n formule te bereken, moet jy die atoommassas van elke teenwoordige element bymekaar tel.
Trappe
Metode 1 van 2: Berekening van die molekulêre massa

1. Tel hoeveel atome van elke element daar in die molekule is. Maak eers `n lys van elke element wat in die molekule teenwoordig is. Jy kan die chemiese simbool gebruik of die naam van die element skryf. Tel dan die atome volgens die molekulêre formule en skryf dit langs die naam of simbool van die element neer.
- Byvoorbeeld: koolstofdioksied of CO2, bevat 1 koolstof (C) en 2 suurstof (O).
- Metaan, CH4, bevat koolstof (C) en waterstof (H). Metaan bestaan uit 1 koolstofatoom en 4 waterstofatome.
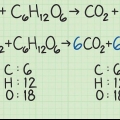
- glukose, CO6huh12O6, bevat koolstof (C), waterstof (H) en suurstof (O). Glukose bestaan uit 6 koolstofatome, 12 waterstofatome en 6 suurstofatome.

2. Besonderrelatiewe atoommassa van elke element in die molekule. Gebruik dit periodieke tabel. Die periodieke tabel lys die atoommassa van elke element onder die chemiese simbool. Byvoorbeeld: suurstof het `n relatiewe atoommassa van 15,9994 amu.

3. Bereken die totale massa van elke element in die molekule. Vermenigvuldig die atoommassa van elke element met die aantal atome van daardie element: (atoommassa van element) x (aantal atome van daardie element). Doen dit vir elke element in die molekule.
 .
.
4. Tel die massas van alle atome by om die molekulêre massa te vind. Molekulêre massa = ∑((atoommassa van die element)n x (aantal atome van daardie element)n)
 .
.Metode 2 van 2: Oefen met voorbeelde

1. Bepaal die molekulêre massa van metaan (CH4). Die atoommassa van waterstof is 1,008 u. Die atoommassa van koolstof is 12 011 u. Daar is vier waterstofatome in metaan. Tel die gewig van alle atome in metaan bymekaar om die molekulêre massa te vind.
.

2. Bereken die molekulêre massa van glukose (C6huh12O6). Die atoommassa van koolstof is 12 011 u. Die atoommassa van waterstof is 1,008 u. Die atoommassa van suurstof is 15 999 Daar is 6 koolstofatome, 12 waterstofatome en 6 suurstofatome. Voeg die massas van al die atome in glukose bymekaar om die molekulêre massa te bereken.




Wenke
- Maak seker jy volg die regte reëls vir betekenisvolle syfers, soos vereis.
Artikels oor die onderwerp "Berekening van molekulêre massa"
Оцените, пожалуйста статью
Soortgelyk
Gewilde